Ang Tofacitinib citrate kay usa ka reseta nga tambal (trade name Xeljanz) nga orihinal nga gimugna ni Pfizer para sa klase sa oral Janus kinase (JAK) inhibitors. Mahimo kini nga pilion nga makapugong sa JAK kinase, makababag sa mga agianan sa JAK / STAT, ug sa ingon makapugong sa transduction sa signal sa cell ug Related gene expression ug activation, nga gigamit sa pagtambal sa rheumatoid arthritis, psoriatic arthritis, ulcerative colitis ug uban pang mga sakit sa immune.
Ang tambal naglakip sa tulo nga mga porma sa dosis: mga papan, mga tablet nga gipadayon nga gipagawas ug mga solusyon sa oral. Ang mga tablet niini unang gi-aprobahan sa FDA niadtong 2012, ug ang sustained-release dosage form gi-aprobahan sa FDA niadtong Pebrero 2016. Kini ang una nga nagtambal sa rheumatoid joints. Ang Yan kay JAK inhibitor nga ginainom kausa sa usa ka adlaw. Niadtong Disyembre 2019, usa ka bag-ong indikasyon alang sa sustained-release nga mga tambal ang giaprobahan pag-usab alang sa kasarangan ngadto sa grabe nga aktibo nga ulcerative colitis (UC). Dugang pa, ang kasamtangan nga hugna 3 clinical mga pagsulay alang sa plake psoriasis nahuman, ug laing unom ka hugna 3 clinical mga pagsulay anaa sa pag-uswag, nga naglakip sa aktibo psoriatic arthritis, juvenile idiopathic arthritis, ug uban pa Matang sa mga timailhan. Ang mga bentaha sa sustained-release nga mga tablet nga dugay nga molihok ug kinahanglan ra nga imnon kausa sa usa ka adlaw makatabang sa pagdumala ug pagpugong sa mga sakit sa mga pasyente.
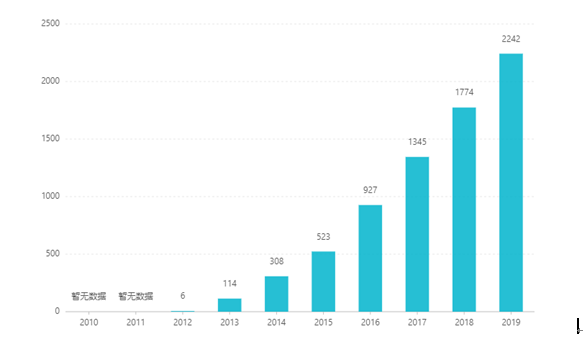
Sukad sa paglista niini, ang halin niini misaka matag tuig, nga moabot sa US$2.242 bilyon sa 2019. Sa China, ang tablet dosage form gi-aprobahan alang sa marketing niadtong Marso 2017, ug misulod sa medical insurance category B catalog pinaagi sa negosasyon sa 2019. Ang pinakabag-o nga kadaugan bid kay RMB 26.79. Bisan pa, tungod sa taas nga teknikal nga mga babag sa padayon nga pagpagawas sa mga pagpangandam, kini nga porma sa dosis wala pa gipamaligya sa China.
Ang JAK kinase adunay importante nga papel sa panghubag, ug ang mga inhibitor niini gipakita sa pagtambal sa pipila ka mga sakit nga makapahubag ug autoimmune. Hangtud karon, 7 nga mga inhibitor sa JAK ang naaprobahan sa tibuok kalibutan, lakip ang Delgocitinib ni Leo Pharma, Fedratinib ni Celgene, upatinib ni AbbVie, Pefitinib ni Astellas, Baritinib ni Eli Lilly Ug Rocotinib ni Novartis. Bisan pa, ang tofacitinib, baritinib ug rocotinib lamang ang gi-aprobahan sa China taliwala sa mga gihisgutan sa ibabaw nga mga tambal. Kami nagpaabut sa Qilu nga "Tofatib Citrate Sustained Release Tablets" nga maaprobahan sa labing dali nga panahon ug makabenepisyo sa daghang mga pasyente.
Sa China, ang orihinal nga panukiduki nga tofacitib citrate gi-aprobahan sa NMPA kaniadtong Marso 2017 alang sa pagtambal sa mga hamtong nga mga pasyente sa RA nga adunay dili igo nga kaepektibo o pagkadili-matugoton sa methotrexate, sa ilawom sa ngalan sa pamatigayon nga Shangjie. Sumala sa datos gikan sa Meinenet, ang pagbaligya sa tofacitib citrate tablets sa mga pampublikong institusyong medikal sa China kaniadtong 2018 mao ang 8.34 milyon nga yuan, nga mas ubos kaysa sa global nga pagbaligya niini. Usa ka dako nga bahin sa hinungdan mao ang presyo. Gikataho nga ang inisyal nga retail nga presyo ni Shangjie kay 2085 yuan (5mg*28 tablets), ug ang binuwan nga gasto kay 4170 yuan, nga dili gamay nga palas-anon alang sa ordinaryong mga pamilya.
Hinuon, angayan nga saulogon nga ang tofacitib nalakip sa 2019 “National Basic Medical Insurance, Work Injury Insurance ug Maternity Insurance Drug List” sa National Medical Insurance Administration human sa negosasyon niadtong Nobyembre 2019. Gikataho nga ang binuwan nga bayronon mokunhod. ngadto sa ubos sa 2,000 yuan human ang pagkunhod sa presyo negosasyon, nga makapauswag pag-ayo sa pagkaanaa sa tambal.
Niadtong Agosto 2018, ang Patent Reexamination Board sa State Intellectual Property Office mihimo sa usa ka review nga desisyon No. 36902 nga hangyo alang sa pagka-invalidation, ug gideklarar nga dili balido ang kinauyokan nga patent sa Pfizertofatib, ang compound patent, tungod sa dili igo nga pagbutyag sa detalye. Bisan pa, ang patente sa Pfizertofatiib nga kristal nga porma (ZL02823587.8, CN1325498C, petsa sa aplikasyon 2002.11.25) matapos sa 2022.
Gipakita sa database sa Insight nga, dugang sa orihinal nga panukiduki, lima ka generic nga tambal sa Chia Tai Tianqing, Qilu, Kelun, Yangtze River, ug Nanjing Chia Tai Tianqing ang giaprobahan alang sa pagpamaligya sa domestic tofacitinib tablet formulations. Bisan pa, alang sa sustained-release nga tipo sa tablet, ang orihinal nga panukiduki nga Pfizer lamang ang nagsumite sa aplikasyon sa pagpamaligya kaniadtong Mayo 26. Ang Qilu mao ang una nga domestic nga kompanya nga nagsumite usa ka aplikasyon sa pagpamaligya alang niini nga pormulasyon. Dugang pa, ang CSPC Ouyi naa sa yugto sa pagsulay sa BE.
Ang Changzhou Pharmaceutical Factory (CPF) usa ka nanguna nga tiggama sa parmasyutiko sa mga API, nahuman ang mga pormulasyon sa China, nga nahimutang sa Changzhou, lalawigan sa Jiangsu. Ang CPF natukod sa 1949. Kami naghalad sa Tofacitinib Citrate gikan sa 2013, ug gisumite na ang DMF. Nakarehistro kami sa daghang mga nasud, ug makasuporta kanimo sa labing kaayo nga suporta sa mga dokumento alang sa Tofacitinib Citrate.
Oras sa pag-post: Hul-23-2021